News Message
DeepMind AlphaFold 4
- by wittx 2026-03-04
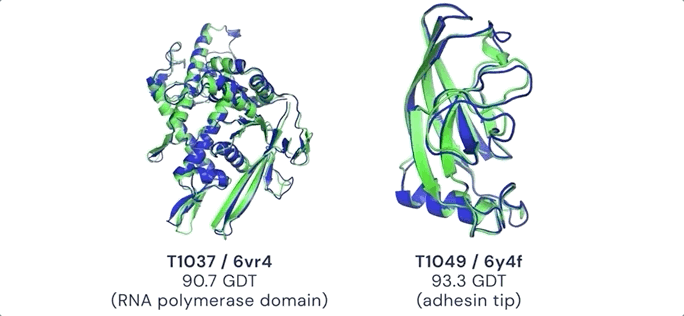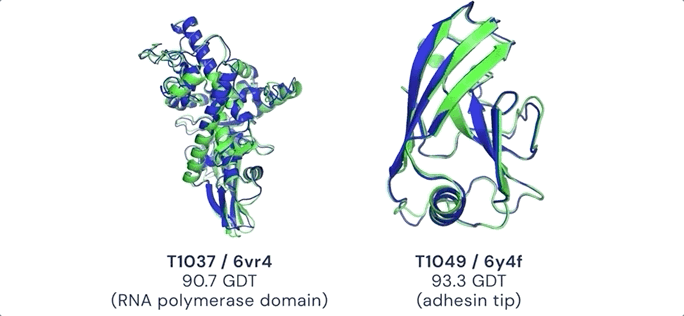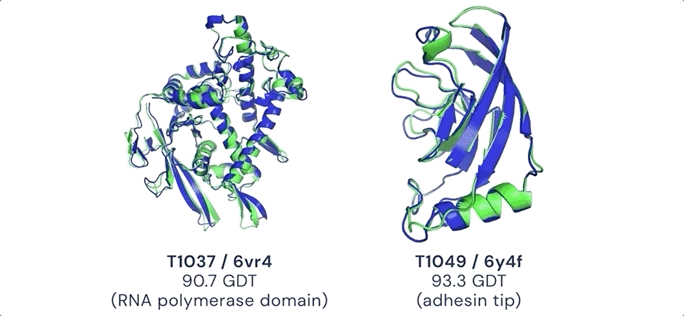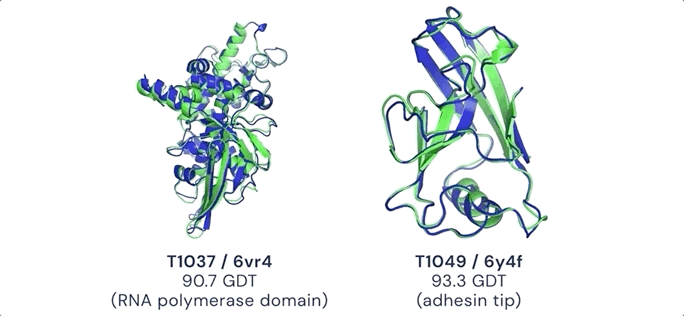
Google DeepMind发布面向药物发现的AlphaFold3近两年后,其生物制药子公司 Isomorphic Labs 再次推出更强大的人工智能模型——但这一次,他们选择完全保密。
这款名为 IsoDDE 的“药物发现引擎”于2月10日通过一份27页技术报告对外公布。报告展示了模型在预测蛋白–药物相互作用以及抗体结构方面的强大能力,引发了计算生物学界的广泛关注。
然而,与此前开放的AlphaFold系列不同,IsoDDE是一款完全专有的闭源系统,技术报告几乎没有透露实现细节。这让许多研究者既震撼又困惑。
一位哥伦比亚大学计算生物学家直言,这项技术是“AlphaFold 4级别的重大突破”,但问题在于,“研究人员几乎不知道它是如何做到的”。

从结构预测走向药物设计
AlphaFold2曾因蛋白结构预测获得诺贝尔奖级影响,而AlphaFold3则进一步扩展到蛋白与小分子、DNA和RNA的复合结构预测,正式进入药物设计领域。
在此基础上,学术界也在快速跟进。例如麻省理工学院团队推出的开源模型 Boltz-2 已能够预测候选药物与蛋白结合的强度(binding affinity)。这一指标是药物研发的关键参数,传统上需要耗费巨大计算资源的物理模拟才能获得。
而Isomorphic的报告宣称:
IsoDDE在结合强度预测上优于Boltz-2
也优于传统物理方法
在抗体–靶点相互作用预测方面同样达到当前最先进水平
如果这些结果成立,意味着AI在药物结构预测领域又向前迈出了一大步。
更令人印象深刻的是,IsoDDE似乎能够预测与训练数据差异很大的新分子与蛋白的相互作用。这被认为是当前最困难的问题之一,因为模型往往会在分布外样本上性能骤降。
“秘密配方”依然保密
Isomorphic Labs总裁表示,IsoDDE背后的模型与现有方法“本质上完全不同”。但公司并不打算公开核心技术。
他表示,突破来自三个因素的结合:
超大规模算力
海量数据
新算法设计
公司希望公开的技术报告能够激励其他团队继续推动药物AI发展,但不会披露关键实现细节。
一些业内研究者猜测,IsoDDE的性能提升可能部分来自企业合作获得的私有结构数据。不过也有研究人员认为,仅凭公开数据仍有大量改进空间。
Google DeepMind发布面向药物发现的AlphaFold3近两年后,其生物制药子公司 Isomorphic Labs 再次推出更强大的人工智能模型——但这一次,他们选择完全保密。
这款名为 IsoDDE 的“药物发现引擎”于2月10日通过一份27页技术报告对外公布。报告展示了模型在预测蛋白–药物相互作用以及抗体结构方面的强大能力,引发了计算生物学界的广泛关注。
然而,与此前开放的AlphaFold系列不同,IsoDDE是一款完全专有的闭源系统,技术报告几乎没有透露实现细节。这让许多研究者既震撼又困惑。
一位哥伦比亚大学计算生物学家直言,这项技术是“AlphaFold 4级别的重大突破”,但问题在于,“研究人员几乎不知道它是如何做到的”。

从结构预测走向药物设计
AlphaFold2曾因蛋白结构预测获得诺贝尔奖级影响,而AlphaFold3则进一步扩展到蛋白与小分子、DNA和RNA的复合结构预测,正式进入药物设计领域。
在此基础上,学术界也在快速跟进。例如麻省理工学院团队推出的开源模型 Boltz-2 已能够预测候选药物与蛋白结合的强度(binding affinity)。这一指标是药物研发的关键参数,传统上需要耗费巨大计算资源的物理模拟才能获得。
而Isomorphic的报告宣称:
IsoDDE在结合强度预测上优于Boltz-2
也优于传统物理方法
在抗体–靶点相互作用预测方面同样达到当前最先进水平
如果这些结果成立,意味着AI在药物结构预测领域又向前迈出了一大步。
更令人印象深刻的是,IsoDDE似乎能够预测与训练数据差异很大的新分子与蛋白的相互作用。这被认为是当前最困难的问题之一,因为模型往往会在分布外样本上性能骤降。
“秘密配方”依然保密
Isomorphic Labs总裁表示,IsoDDE背后的模型与现有方法“本质上完全不同”。但公司并不打算公开核心技术。
他表示,突破来自三个因素的结合:
超大规模算力
海量数据
新算法设计
公司希望公开的技术报告能够激励其他团队继续推动药物AI发展,但不会披露关键实现细节。
一些业内研究者猜测,IsoDDE的性能提升可能部分来自企业合作获得的私有结构数据。不过也有研究人员认为,仅凭公开数据仍有大量改进空间。
Share Http URL: http://www.wittx.cn/get_news_message.do?new_id=1534

Best Last Month


.jpg)